作者:阿华所 摄影:王壮
近日,美国免疫学会会刊《Journal of Immunology》在线报道了我校生物反应器工程国家重点实验室刘琴教授课题组在细胞焦亡调控脓毒症急性肾损伤发生分子机制方面的新成果。
急性肾脏损伤(Acute kidney injury,AKI)是造成脓毒症患者死亡的关键因素,然而,国际上对脓毒性AKI发病机制的解析仍然是重症医学和肾脏病学研究的热点和难点,因此,系统研究脓毒症导致肾脏损伤的关键信号,对于解析脓毒症AKI发生的病理生理特性具有重要意义。细胞焦亡是近十年来被发现并证实的一种新的程序性细胞死亡方式,其调控感染性疾病发生的分子机制是当前国际研究的前沿热点。当机体受到系统性感染,革兰氏阴性细菌的内毒素作为激活细胞焦亡的关键分子,是引发脓毒性休克的关键因素之一,但是,由感染导致的过度细胞焦亡信号如何调控宿主全身炎症反应综合症并引发AKI仍然有待解析。
针对这一挑战,课题组依托模式动物斑马鱼为研究对象,采用细菌突变体文库感染高通量筛选技术,获得了激活鱼类细胞焦亡模型(Cellular Microbiology 2019,封面论文),并阐明了调控鱼类细胞焦亡的关键炎症性caspase(Nature Communications 2018)。在此基础上,课题组进一步建立了实验鱼反向遗传筛选手段,通过CRISPR/cas9快速筛选技术,发现了Caspy2和GSDMEb基因缺失能够缓解致死剂量LPS导致的实验鱼脓毒性休克。通过结构特征、亚细胞定位及其在先天免疫信号通路中的功能发现,GSDME蛋白能够被激活的Caspy2切割,产生的GSDMEb-N端片段多聚化,并在细胞膜上穿孔,导致鱼类细胞焦亡。
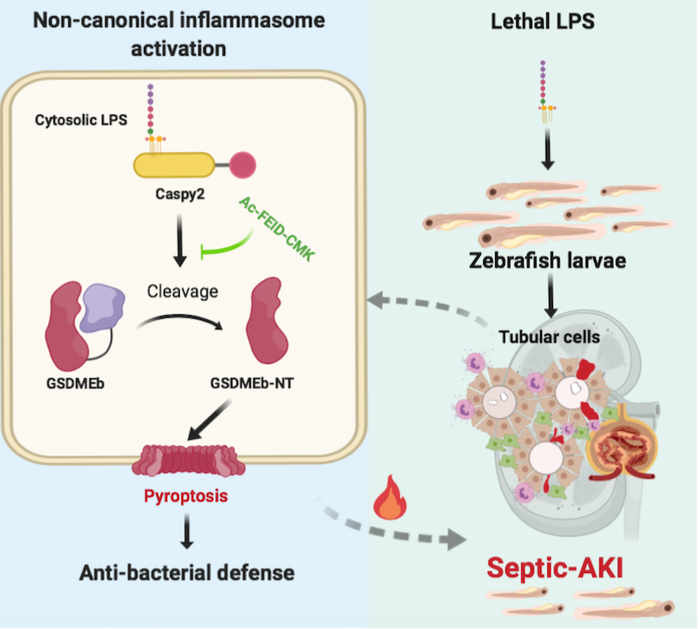
进一步,基于实验鱼活体脓毒性休克模型,立足细胞焦亡信号调控分子的系统筛选,课题组从脓毒症AKI发生的病理生理特性角度出发,深入解析了引发肾小管细胞焦亡的关键分子,发现Caspy2-GSDMEb介导的鱼类肾小管上皮细胞焦亡是引发脓毒症急性肾损伤的关键。并且,在小鼠活体模型上,验证了细胞焦亡信号调控脓毒症AKI的关键指标。据此,课题组设计了斑马鱼GSDMEb切割位点的竞争性肽抑制剂Ac-FEID-CMK,在活体水平上明确了该焦亡信号通路抑制剂能够有效缓解鱼体脓毒症AKI及鱼体死亡。这一成果从活体水平阐明了细胞焦亡信号调控脓毒症AKI发生的分子机制,不仅解析了鱼类细胞焦亡信号通路为代表的固有免疫系统的演化规律,也为重症脓毒性AKI患者的临床诊疗提供理论依据,为开发具有选择性的治疗脓毒症AKI药物提供新的研究策略。
6165cc金沙总站博士研究生王壮是该论文的第一作者,阳大海副教授是通讯作者。该工作得到了东部战区总医院、国家肾脏病临床医学研究中心刘志红院士团队的悉心指导与帮助。研究得到了团队张元兴、刘琴和王启要教授的大力支持。该工作由国家自然科学基金委、中国科协第二批青年人才托举工程等科研项目资助完成。
论文链接:https://www.jimmunol.org/content/204/7/1929?from=singlemessage&isappinstalled=0